중성자, 양성자, 전자의 질량을 amu(원자 질량 단위)로 나타내면 다음과 같습니다:
- **중성자 (Neutron)**: 약 1.008665 amu
- **양성자 (Proton)**: 약 1.007276 amu
- **전자 (Electron)**: 약 0.000549 amu
이 값들은 상대적인 질량을 기준으로 하며, 원자 물리학에서 매우 중요한 역할을 합니다.
# 1 amu(원자 질량 단위)의 질량 유도 과정
원자 질량 단위(amu)는 원자나 분자의 질량을 표현하기 위해 사용하는 단위로, 주로 화학과 물리학에서 널리 사용됩니다. 1 amu는 탄소-12 동위원소(¹²C)의 질량을 기준으로 정의됩니다.
## 정의
1 amu는 탄소-12 원자 1개의 질량의 1/12로 정의됩니다. 즉,
\[
1 \, \text{amu} = \frac{\text{탄소-12 원자 1개의 질량}}{12}
\]

## 질량 유도 과정
### 1. 탄소-12의 질량
탄소-12 원자 1개의 질량은 실험적으로 측정된 값으로, 약 \( 1.992646 \times 10^{-23} \, \text{g} \)입니다. 이 값은 아보가드로 수(1몰당 입자 수, \( N_A = 6.02214076 \times 10^{23} \, \text{mol}^{-1} \))와 몰 질량(12 g/mol)을 이용해 계산할 수 있습니다.
\[
\text{탄소-12 원자 1개의 질량} = \frac{\text{탄소-12의 몰 질량}}{N_A} = \frac{12 \, \text{g/mol}}{6.02214076 \times 10^{23} \, \text{mol}^{-1}} \approx 1.992646 \times 10^{-23} \, \text{g}
\]
### 2. 1 amu 계산
1 amu는 탄소-12 원자 질량의 1/12이므로:
\[
1 \, \text{amu} = \frac{1.992646 \times 10^{-23} \, \text{g}}{12} \approx 1.660539 \times 10^{-24} \, \text{g}
\]
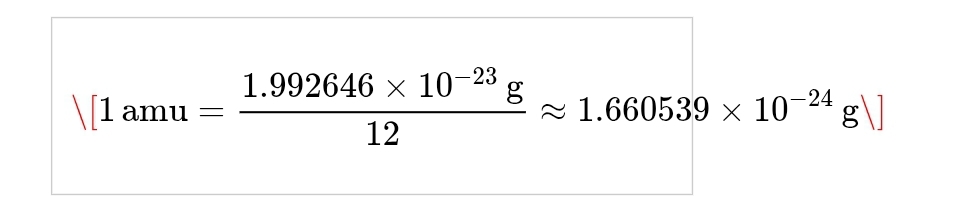
### 3. kg 단위로 변환
1 g는 \( 10^{-3} \, \text{kg} \)이므로:
\[
1 \, \text{amu} \approx 1.660539 \times 10^{-24} \, \text{g} \times 10^{-3} \, \text{kg/g} = 1.660539 \times 10^{-27} \, \text{kg}
\]
## 최종 결과
따라서 1 amu의 질량은 다음과 같습니다:
\[
1 \, \text{amu} \approx 1.660539 \times 10^{-27} \, \text{kg}
\]
이 값은 현대 물리학에서 널리 사용되는 상수이며, 원자 질량을 kg 단위로 표현할 때 유용합니다. 추가 질문이 있다면 언제든지 말씀해 주세요!
유도식 정리
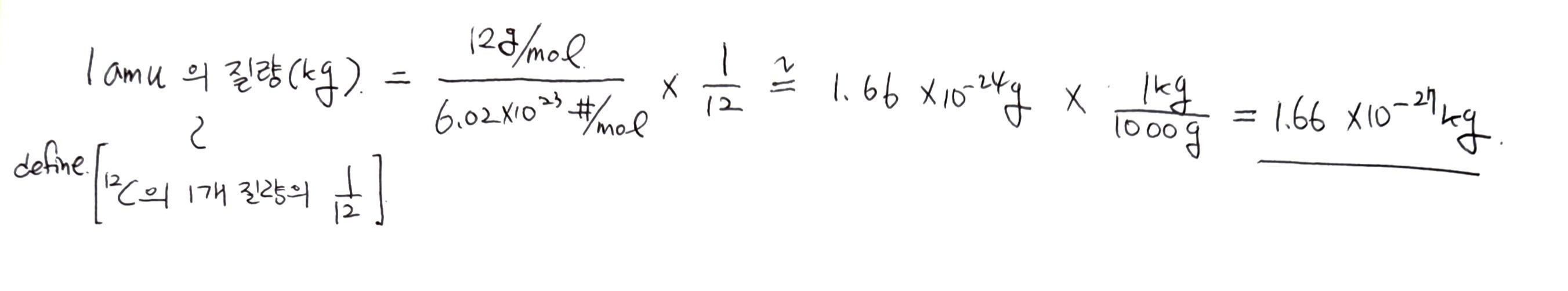
식들을 제대로 보시려면 변환기에 접속해주세요
https://latextohtmlconvertor.netlify.app/
LaTeX to HTML 변환기 convertor
latextohtmlconvertor.netlify.app
'핵연료물질취급자 일반면허 > RM_이론' 카테고리의 다른 글
| 원자력안전법의 "허가"와 "지정"의 차이 및 사용후핵연료처리사업 승인 사례 (0) | 2025.03.12 |
|---|---|
| 파산자(feat. 원자력안전법 14조 원자력관계사업자의 '결격사유') (0) | 2025.03.09 |
| 컴프턴 효과에 대한 이해 🌌 (0) | 2025.03.08 |
| 핵임계안전지수(KI)와 운반제한갯수에 대한 이해 🌟 (1) | 2025.03.07 |
| 태양내부에 수많은 중성자는 왜 지구까지 오지 못할까?! (0) | 2025.03.03 |